Alle FAQ zu Hygiene
DIN 10524 ist eine deutsche Norm, die sich mit der Lebensmittelhygiene in der Gastronomie beschäftigt, speziell im Bereich der Gemeinschaftsverpflegung. Die Norm gibt Anforderungen und Empfehlungen für die hygienische Gestaltung und den Betrieb von Großküchen und Einrichtungen zur Gemeinschaftsverpflegung vor.
Die wichtigsten Aspekte von DIN 10524 sind:
- Hygienische Gestaltung und Ausstattung:
- Anforderungen an die bauliche Gestaltung und die Ausstattung von Küchen und Verpflegungseinrichtungen, um eine einfache Reinigung und Desinfektion zu ermöglichen.
- Vorgaben zur Trennung von reinen und unreinen Bereichen, um Kreuzkontaminationen zu vermeiden.
- Personalhygiene:
- Schulungen und Unterweisungen des Personals in Hygienemaßnahmen und -praktiken.
- Vorgaben zur persönlichen Hygiene der Mitarbeiter, einschließlich Kleidung, Handhygiene und Verhalten im Umgang mit Lebensmitteln.
- Hygienemanagement:
- Entwicklung und Umsetzung eines Hygienekonzepts, das auf den Prinzipien des HACCP-Systems basiert.
- Dokumentation und Überwachung der Hygienemaßnahmen, um deren Einhaltung sicherzustellen.
- Lebensmittelhygiene:
- Anforderungen an den Umgang mit Lebensmitteln, von der Anlieferung über die Lagerung bis zur Zubereitung und Ausgabe.
- Maßnahmen zur Vermeidung von Kontaminationen und zur Sicherstellung der Lebensmittelsicherheit.
- Reinigung und Desinfektion:
- Vorgaben zur regelmäßigen und systematischen Reinigung und Desinfektion von Räumen, Geräten und Arbeitsflächen.
- Verwendung geeigneter Reinigungs- und Desinfektionsmittel.
- Abfallmanagement:
- Hygienische Entsorgung von Abfällen, um Verunreinigungen und Schädlinge zu vermeiden.
- Anforderungen an Abfallbehälter und deren Handhabung.
- Wartung und Instandhaltung:
- Regelmäßige Wartung und Instandhaltung von technischen Einrichtungen und Geräten, um deren einwandfreien hygienischen Zustand sicherzustellen.
DIN 10524 dient dazu, ein hohes Maß an Lebensmittelsicherheit und Hygiene in Gemeinschaftsverpflegungseinrichtungen zu gewährleisten. Sie hilft dabei, die Risiken von lebensmittelbedingten Krankheiten zu minimieren und die Qualität der angebotenen Speisen zu sichern. Die Norm ist für alle Arten von Einrichtungen relevant, die regelmäßig eine große Anzahl von Menschen mit Mahlzeiten versorgen, wie z.B. Kantinen, Mensen, Krankenhäuser und Altenheime.
- Hygienische Gestaltung und Ausstattung:
Das HACCP-Konzept wird in einer Vielzahl von Branchen umgesetzt, die mit der Produktion, Verarbeitung, Lagerung und dem Vertrieb von Lebensmitteln und Getränken befasst sind. Zu den Hauptbranchen, die das HACCP-Konzept anwenden, gehören:
- Lebensmittelverarbeitende Industrie:
- Fleisch- und Geflügelverarbeitung: Schlachthöfe, Fleischverarbeitungsbetriebe und Hersteller von Wurstwaren.
- Fisch- und Meeresfrüchteverarbeitung: Fischereien, Fischverarbeitungsbetriebe und Hersteller von Meeresfrüchteprodukten.
- Milch- und Molkereiprodukte: Molkereien, Käsehersteller und Produzenten von Joghurt und anderen Milchprodukten.
- Backwaren und Süßwaren: Bäckereien, Konditoreien und Hersteller von Süßwaren.
- Fertiggerichte und Convenience-Produkte: Hersteller von vorgefertigten Mahlzeiten und Tiefkühlprodukten.
- Getränkeindustrie: Abfüller und Hersteller von alkoholfreien und alkoholischen Getränken, einschließlich Wasserabfüller und Brauereien.
- Landwirtschaft und Primärproduktion:
- Landwirtschaftliche Betriebe: Erzeuger von Obst, Gemüse, Getreide und anderen landwirtschaftlichen Produkten.
- Tierhaltung und Viehzucht: Betriebe, die Tiere für die Fleisch-, Milch- und Eierproduktion halten.
- Gastronomie und Lebensmittelservice:
- Restaurants und Cafés: Einrichtungen, die Speisen und Getränke für den Verzehr vor Ort oder zum Mitnehmen anbieten.
- Catering-Unternehmen: Unternehmen, die Speisen und Getränke für Veranstaltungen und Firmen liefern.
- Kantinen und Großküchen: Küchen in Schulen, Krankenhäusern, Unternehmen und anderen Einrichtungen, die eine große Anzahl von Menschen versorgen.
- Einzelhandel und Vertrieb:
- Supermärkte und Lebensmittelgeschäfte: Einzelhandelsgeschäfte, die eine Vielzahl von frischen und verarbeiteten Lebensmitteln verkaufen.
- Großhändler und Distributoren: Unternehmen, die Lebensmittel in großen Mengen lagern und an Einzelhändler und andere Kunden verteilen.
- Logistik und Lagerung:
- Kühl- und Lagerhäuser: Einrichtungen, die Lebensmittel unter kontrollierten Bedingungen lagern, um deren Haltbarkeit zu gewährleisten.
- Transport- und Logistikunternehmen: Unternehmen, die für den sicheren Transport von Lebensmitteln verantwortlich sind, einschließlich temperaturgesteuerter Transporte.
- Verpackungsindustrie:
- Lebensmittelverpackungshersteller: Unternehmen, die Verpackungen für Lebensmittel herstellen, um deren Sicherheit und Haltbarkeit zu gewährleisten.
Die Implementierung des HACCP-Konzepts in diesen Branchen hilft dabei, potenzielle Gefahren in der gesamten Lebensmittelkette zu identifizieren und zu kontrollieren, um die Sicherheit und Qualität der Lebensmittel zu gewährleisten.
- Lebensmittelverarbeitende Industrie:
In der Lebensmittelsicherheit werden Lebensmittel je nach ihrer Anfälligkeit für mikrobiologische Gefahren und anderen Risikofaktoren in verschiedene Risikoklassen eingeteilt. Diese Risikoklassen helfen dabei, die notwendigen Kontrollen und Sicherheitsmaßnahmen zu definieren. Die drei häufigsten Risikoklassen sind:
- Risikoklasse I: Lebensmittel mit hohem Risiko
- Diese Lebensmittel haben ein hohes Potenzial für mikrobiologische Kontamination und können bei unsachgemäßer Handhabung oder Verarbeitung schwerwiegende gesundheitliche Probleme verursachen.
- Beispiele: Rohe Meeresfrüchte, rohe Eier, nicht pasteurisierte Milchprodukte, rohes Geflügel, Fleischprodukte und vorgekochte, kühl gelagerte Lebensmittel.
- Erforderliche Maßnahmen: Strenge Überwachungs- und Kontrollverfahren, Temperaturkontrollen, gute Hygienepraxis (GHP) und umfassende Schulung der Mitarbeiter.
- Risikoklasse II: Lebensmittel mit mittlerem Risiko
- Diese Lebensmittel haben ein moderates Risiko für Kontamination und können unter bestimmten Bedingungen gesundheitliche Probleme verursachen.
- Beispiele: Frisches Obst und Gemüse, Brot und Backwaren, verpackte und gekühlte Lebensmittel, die keine spezifische Zubereitung erfordern.
- Erforderliche Maßnahmen: Regelmäßige Kontrollen und Inspektionen, Einhaltung der Lagerungstemperaturen und Hygienepraktiken.
- Risikoklasse III: Lebensmittel mit geringem Risiko
- Diese Lebensmittel haben ein geringes Potenzial für mikrobiologische Kontamination und sind in der Regel sicher, wenn sie unter normalen Bedingungen gelagert und gehandhabt werden.
- Beispiele: Getreideprodukte, Konserven, trockene Lebensmittel wie Nudeln und Reis, nicht verderbliche, abgepackte Lebensmittel.
- Erforderliche Maßnahmen: Grundlegende Hygienemaßnahmen und Einhaltung der Lagerungsvorschriften.
Diese Risikoklassen dienen als Leitfaden für die Entwicklung und Umsetzung von HACCP-Plänen sowie anderen Lebensmittelsicherheitsmaßnahmen. Sie helfen dabei, die Ressourcen und Anstrengungen auf die Bereiche zu konzentrieren, die das höchste Risiko für die Gesundheit der Verbraucher darstellen.
- Risikoklasse I: Lebensmittel mit hohem Risiko
HACCP wird umgesetzt, um die Sicherheit von Lebensmitteln zu gewährleisten und das Risiko von lebensmittelbedingten Krankheiten und Kontaminationen zu minimieren.
Konkret dient die Umsetzung von HACCP folgenden Zwecken:
- Schutz der Verbraucher: Durch die Identifizierung und Kontrolle potenzieller Gefahren soll sichergestellt werden, dass die Lebensmittel sicher für den Verzehr sind. Dies schützt die Gesundheit der Verbraucher vor Krankheiten und Vergiftungen.
- Einhaltung gesetzlicher Vorschriften: In vielen Ländern ist die Implementierung von HACCP-Systemen gesetzlich vorgeschrieben. Lebensmittelunternehmen müssen HACCP anwenden, um den nationalen und internationalen Lebensmittelsicherheitsstandards zu entsprechen.
- Vermeidung von Kontaminationsrisiken: HACCP hilft dabei, Kontaminationsrisiken durch biologische (z.B. Bakterien, Viren), chemische (z.B. Pestizide, Allergene) und physikalische (z.B. Fremdkörper) Gefahren zu minimieren oder zu eliminieren.
- Qualitätssicherung: Neben der Lebensmittelsicherheit trägt HACCP auch zur allgemeinen Qualitätssicherung bei, indem es systematische und dokumentierte Prozesse für die Herstellung und Verarbeitung von Lebensmitteln etabliert.
- Vertrauensbildung: Die Umsetzung eines HACCP-Systems signalisiert den Verbrauchern und Geschäftspartnern, dass das Unternehmen proaktiv Maßnahmen zur Gewährleistung der Lebensmittelsicherheit ergreift. Dies stärkt das Vertrauen in die Marke und das Produkt.
- Wirtschaftliche Vorteile: Durch die Vermeidung von Lebensmittelrückrufen, Schadensersatzansprüchen und Imageverlust können Unternehmen finanzielle Verluste vermeiden. Ein effektives HACCP-System kann zudem die Effizienz der Produktionsprozesse verbessern und Abfälle reduzieren.
- Internationaler Handel: Für Unternehmen, die Lebensmittel exportieren, ist die Einhaltung von HACCP oft eine Voraussetzung, um Zugang zu internationalen Märkten zu erhalten. Viele Importländer verlangen den Nachweis eines funktionierenden HACCP-Systems.
Die Umsetzung von HACCP erfordert die Zusammenarbeit und das Engagement aller Beteiligten im Lebensmittelbetrieb. Es ist ein kontinuierlicher Prozess, der regelmäßige Überprüfungen und Anpassungen verlangt, um den sich ändernden Bedingungen und neuen Erkenntnissen in der Lebensmittelsicherheit gerecht zu werden.
HACCP steht für „Hazard Analysis and Critical Control Points“ und ist ein systematisches Verfahren zur Gewährleistung der Lebensmittelsicherheit. Es zielt darauf ab, potenzielle Gefahren in den verschiedenen Phasen der Lebensmittelproduktion und -verarbeitung zu identifizieren, zu bewerten und zu kontrollieren. HACCP ist ein präventives System, das von der Erzeugung der Rohstoffe bis zur Verteilung des Endprodukts angewendet wird.
Das HACCP-System umfasst sieben grundlegende Prinzipien:
- Gefahrenanalyse: Identifikation von biologischen, chemischen oder physikalischen Gefahren, die den Lebensmitteln schaden könnten.
- Bestimmung der kritischen Kontrollpunkte (CCPs): Festlegung der Punkte im Produktionsprozess, an denen die identifizierten Gefahren kontrolliert werden können.
- Festlegung von Grenzwerten: Definition von Grenzwerten für die jeweiligen kritischen Kontrollpunkte, um sicherzustellen, dass die Gefahren unter Kontrolle bleiben.
- Überwachung der kritischen Kontrollpunkte: Implementierung von Überwachungsverfahren, um sicherzustellen, dass die Grenzwerte eingehalten werden.
- Korrekturmaßnahmen: Festlegung von Maßnahmen, die ergriffen werden müssen, wenn ein kritischer Kontrollpunkt außerhalb der festgelegten Grenzwerte liegt.
- Verifizierung: Bestätigung, dass das HACCP-System ordnungsgemäß funktioniert und die Lebensmittelsicherheit gewährleistet ist.
- Dokumentation und Aufzeichnungen: Führung detaillierter Aufzeichnungen aller Maßnahmen und Verfahren, um die Einhaltung des HACCP-Systems zu belegen.
HACCP ist international anerkannt und wird von vielen Lebensmittelunternehmen weltweit implementiert, um die Sicherheit ihrer Produkte zu gewährleisten. Es ist oft ein gesetzlich vorgeschriebenes System, insbesondere in der Europäischen Union und den USA.
Die Implementierung eines HACCP-Systems erfordert Schulungen und das Engagement aller Mitarbeiter im Lebensmittelbetrieb, um effektiv zu sein. Es ist ein dynamischer Prozess, der regelmäßig überprüft und angepasst werden muss, um den sich ändernden Bedingungen und neuen Erkenntnissen in der Lebensmittelsicherheit gerecht zu werden.
Sauerstoff ist überall auf der Erde vorhanden und ohne dieses wichtige Molekül wäre Leben auf der Erde nicht möglich. Wird das Sauerstoffmolekül (O2) energetisch angeregt, entsteht der sogenannte Singulett Sauerstoff (kurz: 1O2, englisch: singlet oxygen). Singulett Sauerstoff kann sehr effizient durch den photodynamischen Mechanismus erzeugt werden.
Singulett Sauerstoff mit antimikrobieller Wirkung
Dieser hochreaktive Singulett Sauerstoff wird seit über 20 Jahren in der Medizin zur Behandlung von Tumoren und degenerativen Erkrankungen routinemäßig eingesetzt. Zeitgleich wurde der antimikrobielle Einsatz von Singulett Sauerstoff entwickelt. Viren, Bakterien und Pilze werden durch diesen hochreaktiven Sauerstoff schnell und effizient zerstört. Eine Resistenzentwicklung, wie sie bei Antibiotika und konventionellen Bioziden zu beobachten ist, tritt bei Singulett Sauerstoff nicht auf.
Nachweisbarkeit der Wirkung von Singulett Sauerstoff
Es gibt derzeit mindestens 34 wissenschaftliche Studien, die beweisen, dass Singulett Sauerstoff auch verschiedenste Viren effizient zerstören kann. Weiter gibt es mehr als Hundert wissenschaftliche Studien, die beweisen, dass Singulett Sauerstoff verschiedenste pathogene Pilze effizient abtöten kann
Diese Studien wurden mit wissenschaftlich standardisierten Methoden durchgeführt und in peer-reviewed Fachjournals publiziert.
Die wissenschaftlichen Studien zeigen, dass Singulett Sauerstoff…
- die Zerstörung der Viren bzw. die Abtötung der Bakterien und Pilze mittels Peroxidation von Lipiden und Proteinen bewirkt
- damit behüllte und unbehüllte Viren effizient zerstört
- häufig auftretende Viren wie Influenzaviren, Herpesviren, Noroviren und HIV zerstört
- hochpathogene Viren wie Ebolaviren und SARS Coronaviren zerstört
- sich als sehr wirksam gegen den weit verbreiteten Hefepilz C. albicans zeigt
- Grampositive und Gramnegative Bakterien gleichermaßen inaktiviert
- Bakterien unabhängig von ihrer Antibiotika-Resistenz inaktiviert
- insbesondere Bakterien der ESKAPE Gruppe inaktiviert
- auch gegen Antimykotika-resistente Pilze wirkt
Keime, deren Inaktivierung durch Singulett Sauerstoff mittels wissenschaftlicher Studien belegt ist
Viren
- bacteriophages
- baculovirus
- bovine enterovirus
- chikungunya virus
- Coronavirus MERS-CoV
- Coronavirus SARS-CoV
- coxsackievirus
- Crimean-Congo haemorrhagic fever virus
- dengue virus
- Ebolavirus
- feline calicivirus
- herpes simplex virus
- hepatitis B
- hepatitis C
- human adenovirus
- human cytomegalovirus
- human immunodeficiency virus
- human norovirus
- infectious hematopoietic necrosis virus
- influenza virus
- mayaro virus
- mouse polyomavirus
- murine norovirus
- Newcastle diseasevirus
- Nipah virus
- Sindbis virus
- vesicular stomatitis virus
- Zika virus
Bakterien
- Acinetobacter baumannii
- Actinomyces naeslundii
- Actinomyces viscosus
- Aggregatibacter actinomycetemcomitans
- Bacillus atrophaeus
- Bacillus subtilis
- Bacteroides thetaiotaomicron
- Campylobacter jejuni
- Clostridium ditficile
- Deinococcus radiodurans
- Enterobacter cloacae
- Enterococcus faecalis
- Enterococcus faeclum
- Escherichia coll
- Fusobacterium nucleatum
- Helicobacter pylori
- Hemophilus influenzae
- Klebsiella oxytoca
- Klebslella pneumonlae
- Listeria monocytogenes
- MDR
- MRSA
- Mycobacterium bovis
- Mycobacterium chelonae
- Porphyromonas gingivalis
- Propionibacterium acnes
- Proteus mirabilis
- Pseudomonas aeruginosa
- Salmonella enterica serovar Typhimurium
- Serratia marcescens
- Staphylococcus aureus
- Staphylococcus epidermidis
- Streptococcus bovis
- Streptococcus mutans
- Streptococcus pneumoniae
- Vibrio parahaemolyticus
- Vibrio vulnificus
- VRE
Pilze
- Aspergillus flavues
- Aspergillus fumigatus
- Aspergillus niger
- Candida albicans
- Candida auris
- Candida dubliniensis
- Candida krusei
- Candida parapsilosis
- Cladosporium cladosporioides
- Colletotrichum graminicola
- Cryptococcus neoformans
- Fusarium oxysporum
- Malassezia spp.
- Penicillium chrysogenum
- Penicillium purpurgenum
- Scopulariopsis brevicaulis
- Saccharomyces cerevisiae
- Trichophyton rubrum
Wissenschaftliche Studien zur antiviralen Wirkung von Singulett Sauerstoff
- Wiehe, A., J.M. O’Brien, and M.O. Senge, Trends and targets in antiviral phototherapy. Photochemical & Photobiological Sciences, 2019. 18(11): p. 2565-2612.
- Hollmann, A., et al., Singlet oxygen effects on lipid membranes: implications for the mechanism of action of broad-spectrum viral fusion inhibitors. Biochemical Journal, 2014. 459: p. 161-170.
- Korneev, D., et al., Ultrastructural Aspects of Photodynamic Inactivation of Highly Pathogenic Avian H5N8 Influenza Virus. Viruses, 2019. 11(10).
- Majiya, H., et al., Photodynamic inactivation of non-enveloped RNA viruses. J Photochem Photobiol B, 2018. 189: p. 87-94.
- Teles, A.V., et al., Photodynamic inactivation of Bovine herpesvirus type 1 (BoHV-1) by porphyrins. J Gen Virol, 2018. 99(9): p. 1301-1306.
- Cruz-Oliveira, C., et al., Mechanisms of Vesicular Stomatitis Virus Inactivation by Protoporphyrin IX, Zinc-Protoporphyrin IX, and Mesoporphyrin IX. Antimicrob Agents Chemother, 2017. 61(6).
- Balmer, B.F., et al., Inhibition of an Aquatic Rhabdovirus Demonstrates Promise of a Broad-Spectrum Antiviral for Use in Aquaculture. Journal of Virology, 2017. 91(4).
- Carpenter, B.L., et al., Antiviral, Antifungal and Antibacterial Activities of a BODIPY-Based Photosensitizer. Molecules, 2015. 20(6): p. 10604-10621.
- Ke, M.R., et al., Photodynamic inactivation of bacteria and viruses using two monosubstituted zinc(II) phthalocyanines. European Journal of Medicinal Chemistry, 2014. 84: p. 278-283.
- Verhaelen, K., et al., Wipes Coated with a Singlet-Oxygen-Producing Photosensitizer Are Effective against Human Influenza Virus but Not against Norovirus. Applied and Environmental Microbiology, 2014. 80(14): p. 4391-4397.
- Vigant, F., et al., The Rigid Amphipathic Fusion Inhibitor dUY11 Acts through Photosensitization of Viruses. Journal of Virology, 2014. 88(3): p. 1849-1853.
- Rosado-Lausell, S.L., et al., Roles of singlet oxygen and triplet excited state of dissolved organic matter formed by different organic matters in bacteriophage MS2 inactivation. Water Research, 2013. 47(14): p. 4869-4879.
- Vigant, F., et al., A Mechanistic Paradigm for Broad-Spectrum Antivirals that Target Virus-Cell Fusion. Plos Pathogens, 2013. 9(4).
- Costa, L., et al., Involvement of type I and type II mechanisms on the photoinactivation of non-enveloped DNA and RNA bacteriophages. J Photochem Photobiol B, 2013. 120: p. 10-6.
- Lhotakova, Y., et al., Virucidal nanofiber textiles based on photosensitized production of singlet oxygen. PLoS One, 2012. 7(11): p. e49226.
- Rule Wigginton, K., et al., Oxidation of virus proteins during UV(254) and singlet oxygen mediated inactivation. Environ Sci Technol, 2010. 44(14): p. 5437-43.
- Hotze, E.M., et al., Mechanisms of bacteriophage inactivation via singlet oxygen generation in UV illuminated fullerol suspensions. Environ Sci Technol, 2009. 43(17): p. 6639-45.
- Wen, W.H., et al., Synergistic effect of zanamivir-porphyrin conjugates on inhibition of neuraminidase and inactivation of influenza virus. J Med Chem, 2009. 52(15): p. 4903-10.
- Tome, J.P., et al., Synthesis of neutral and cationic tripyridylporphyrin-D-galactose conjugates and the photoinactivation of HSV-1. Bioorg Med Chem, 2007. 15(14): p. 4705-13.
- Mohr, H., et al., Virus inactivation of blood products by phenothiazine dyes and light. Photochem Photobiol, 1997. 65(3): p. 441-5.
- Hirayama, J., et al., Involvement of reactive oxygen species in hemoglobin oxidation and virus inactivation by 1,9-dimethylmethylene blue phototreatment. Biol Pharm Bull, 2001. 24(4): p. 418-21.
- Lin, Y.L., et al., Light-independent inactivation of dengue-2 virus by carboxyfullerene C3 isomer. Virology, 2000. 275(2): p. 258-62.
- Pellieux, C., et al., Bactericidal and virucidal activities of singlet oxygen generated by thermolysis of naphthalene endoperoxides. Methods Enzymol, 2000. 319: p. 197-207.
- Stroop, W.G., et al., PCR assessment of HSV-1 corneal infection in animals treated with rose bengal and lissamine green B. Invest Ophthalmol Vis Sci, 2000. 41(8): p. 2096-102.
- Yip, L., et al., Antiviral activity of a derivative of the photosensitive compound Hypericin. Phytomedicine, 1996. 3(2): p. 185-90.
- Lenard, J., A. Rabson, and R. Vanderoef, Photodynamic inactivation of infectivity of human immunodeficiency virus and other enveloped viruses using hypericin and rose bengal: inhibition of fusion and syncytia formation. Proc Natl Acad Sci U S A, 1993. 90(1): p. 158-62.
- Neris, R.L.S., et al., Co-protoporphyrin IX and Sn-protoporphyrin IX inactivate Zika, Chikungunya and other arboviruses by targeting the viral envelope. Scientific Reports, 2018. 8.
- Randazzo, W., R. Aznar, and G. Sanchez, Curcumin-Mediated Photodynamic Inactivation of Norovirus Surrogates. Food Environ Virol, 2016. 8(4): p. 244-250.
- Latief, M.A., et al., Inactivation of acyclovir-sensitive and -resistant strains of herpes simplex virus type 1 in vitro by photodynamic antimicrobial chemotherapy. Mol Vis, 2015. 21: p. 532-7.
- Banerjee, I., et al., Light-activated nanotube-porphyrin conjugates as effective antiviral agents. Nanotechnology, 2012. 23(10).
- Lim, M.E., et al., Photodynamic inactivation of viruses using upconversion nanoparticles. Biomaterials, 2012. 33(6): p. 1912-1920.
- Yin, H.J., et al., Photoinactivation of cell-free human immunodeficiency virus by hematoporphyrin monomethyl ether. Lasers in Medical Science, 2012. 27(5): p. 943-950.
- Costa, L., et al., Evaluation of resistance development and viability recovery by a non-enveloped virus after repeated cycles of aPDT. Antiviral Research, 2011. 91(3): p. 278-282.
- Eickmann, M., et al., Inactivation of Ebola virus and Middle East respiratory syndrome coronavirus in platelet concentrates and plasma by ultraviolet C light and methylene blue plus visible light, respectively. Transfusion, 2018. 58(9): p. 2202-2207.
Wissenschaftliche Studien zur antibakteriellen Wirkung von Singulett Sauerstoff
- Nie, X., et al., Carbon quantum dots: A bright future as photosensitizers for in vitro antibacterial photodynamic inactivation. J Photochem Photobiol B, 2020. 206: p. 111864.
- Mlynarczyk, D.T., et al., Tribenzoporphyrazines with dendrimeric peripheral substituents and their promising photocytotoxic activity against Staphylococcus aureus. Journal of Photochemistry and Photobiology B-Biology, 2020. 204.
- Revuelta-Maza, M.A., et al., Fluorine-substituted tetracationic ABAB-phthalocyanines for efficient photodynamic inactivation of Gram-positive and Gram-negative bacteria. European Journal of Medicinal Chemistry, 2020. 187.
- Santos, D.D., et al., A novel technique of antimicrobial photodynamic therapy – aPDT using 1,9-dimethyl-methylene blue zinc chloride double salt-DMMB and polarized light on Staphylococcus aureus. Journal of Photochemistry and Photobiology B-Biology, 2019. 200.
- Ballatore, M.B., et al., Bacteriochlorin-bis(spermine) conjugate affords an effective photodynamic action to eradicate microorganisms. Journal of Biophotonics, 2020. 13(2).
- Yao, T.T., et al., A photodynamic antibacterial spray-coating based on the host-guest immobilization of the photosensitizer methylene blue. Journal of Materials Chemistry B, 2019. 7(33): p. 5089-5095.
- Chen, W.F., et al., Wool/Acrylic Blended Fabrics as Next-Generation Photodynamic Antimicrobial Materials. Acs Applied Materials & Interfaces, 2019. 11(33): p. 29557-29568.
- Heredia, D.A., et al., Antimicrobial Photodynamic Polymeric Films Bearing Biscarbazol Triphenylamine End-Capped Dendrimeric Zn(II) Porphyrin. Acs Applied Materials & Interfaces, 2019. 11(31): p. 27574-27587.
- Agazzi, M.L., et al., Light-Harvesting Antenna and Proton-Activated Photodynamic Effect of a Novel BODIPY-Fullerene C-60 Dyad as Potential Antimicrobial Agent. Chemphyschem, 2019. 20(9): p. 1110-1125.
- Huang, L.Y., et al., Comparison of two functionalized fullerenes for antimicrobial photodynamic inactivation: Potentiation by potassium iodide and photochemical mechanisms. Journal of Photochemistry and Photobiology B-Biology, 2018. 186: p. 197-206.
- Wang, J., et al., Visible light-induced biocidal activities and mechanistic study of neutral porphyrin derivatives against S-aureus and E. coli. Journal of Photochemistry and Photobiology B-Biology, 2018. 185: p. 199-205.
- Bresoli-Obach, R., et al., Triphenylphosphonium cation: A valuable functional group for antimicrobial photodynamic therapy. J Biophotonics, 2018. 11(10): p. e201800054.
- Cieplik, F., et al., Phenalen-1-one-Mediated Antimicrobial Photodynamic Therapy: Antimicrobial Efficacy in a Periodontal Biofilm Model and Flow Cytometric Evaluation of Cytoplasmic Membrane Damage. Front Microbiol, 2018. 9: p. 688.
- Li, C., et al., Self-Assembled Rose Bengal-Exopolysaccharide Nanoparticles for Improved Photodynamic Inactivation of Bacteria by Enhancing Singlet Oxygen Generation Directly in the Solution. ACS Appl Mater Interfaces, 2018. 10(19): p. 16715-16722.
- Hynek, J., et al., Designing Porphyrinic Covalent Organic Frameworks for the Photodynamic Inactivation of Bacteria. ACS Appl Mater Interfaces, 2018. 10(10): p. 8527-8535.
- de Annunzio, S.R., et al., Susceptibility of Enterococcus faecalis and Propionibacterium acnes to antimicrobial photodynamic therapy. J Photochem Photobiol B, 2018. 178: p. 545-550.
- Zhou, W., et al., High Antimicrobial Activity of Metal-Organic Framework-Templated Porphyrin Polymer Thin Films. ACS Appl Mater Interfaces, 2018. 10(2): p. 1528-1533.
- Huang, L.Y., et al., Potentiation by potassium iodide reveals that the anionic porphyrin TPPS4 is a surprisingly effective photosensitizer for antimicrobial photodynamic inactivation. Journal of Photochemistry and Photobiology B-Biology, 2018. 178: p. 277-286.
- Muller, A., A. Preuss, and B. Roder, Photodynamic inactivation of Escherichia coli – Correlation of singlet oxygen kinetics and phototoxicity. J Photochem Photobiol B, 2018. 178: p. 219-227.
- Eckl, D.B., et al., A Closer Look at Dark Toxicity of the Photosensitizer TMPyP in Bacteria. Photochemistry and Photobiology, 2018. 94(1): p. 165-172.
- Yoshida, A., et al., Antimicrobial effect of blue light using Porphyromonas gingivalis pigment. Scientific Reports, 2017. 7.
- Skwor, T.A., et al., Photodynamic inactivation of methicillin-resistant Staphylococcus aureus and Escherichia coli: A metalloporphyrin comparison. Journal of Photochemistry and Photobiology B-Biology, 2016. 165: p. 51-57.
- Ishiyama, K., et al., Bactericidal Action of Photodynamic Antimicrobial Chemotherapy (PACT) with Photosensitizers Used as Plaque-Disclosing Agents against Experimental Biofilm. Biocontrol Sci, 2016. 21(3): p. 187-91.
- Silva, Z.S., Jr., et al., Papain gel containing methylene blue for simultaneous caries removal and antimicrobial photoinactivation against Streptococcus mutans biofilms. Sci Rep, 2016. 6: p. 33270.
- Wu, J., et al., Photodynamic effect of curcumin on Vibrio parahaemolyticus. Photodiagnosis Photodyn Ther, 2016. 15: p. 34-9.
- Maraccini, P.A., J. Wenk, and A.B. Boehm, Photoinactivation of Eight Health-Relevant Bacterial Species: Determining the Importance of the Exogenous Indirect Mechanism. Environ Sci Technol, 2016. 50(10): p. 5050-9.
- Ruiz-Gonzalez, R., et al., A Comparative Study on Two Cationic Porphycenes: Photophysical and Antimicrobial Photoinactivation Evaluation. Int J Mol Sci, 2015. 16(11): p. 27072-86.
Wissenschaftliche Studien zur antifungalen Wirkung von Singulett Sauerstoff
- Mlynarczyk, D.T., et al., Tribenzoporphyrazines with dendrimeric peripheral substituents and their promising photocytotoxic activity against Staphylococcus aureus. Journal of Photochemistry and Photobiology BBiology, 2020. 204.
- Ballatore, M.B., et al., Bacteriochlorin-bis(spermine) conjugate affords an effective photodynamic action to eradicate microorganisms. Journal of Biophotonics, 2020. 13(2).
- Huang, L.Y., et al., Comparison of two functionalized fullerenes for antimicrobial photodynamic inactivation: Potentiation by potassium iodide and photochemical mechanisms. Journal of Photochemistry and Photobiology B-Biology, 2018. 186: p. 197-206.
- Huang, L.Y., et al., Potentiation by potassium iodide reveals that the anionic porphyrin TPPS4 is a surprisingly effective photosensitizer for antimicrobial photodynamic inactivation. Journal of Photochemistry and Photobiology B-Biology, 2018. 178: p. 277-286.
- Huang, L.Y., et al., Stable synthetic mono-substituted cationic bacteriochlorins mediate selective broadspectrum photoinactivation of drug-resistant pathogens at nanomolar concentrations. Journal of Photochemistry and Photobiology B-Biology, 2014. 141: p. 119-127.
- Vilsinski, B.H., et al., Formulation of Aluminum Chloride Phthalocyanine in Pluronic (TM) P-123 and F-127 Block Copolymer Micelles: Photophysical properties and Photodynamic Inactivation of Microorganisms. Photochemistry and Photobiology, 2015. 91(3): p. 518-525.
- Chibebe, J., et al., Selective photoinactivation of Candida albicans in the non-vertebrate host infection model Galleria mellonella. Bmc Microbiology, 2013. 13.
- Andreazza, N.L., et al., Photodynamic Inactivation of Yeast and Bacteria by Extracts of Alternanthera brasiliana. Current Drug Targets, 2013. 14(9): p. 1015-1022.
- Prates, R.A., et al., Effect of Virulence Factors on the Photodynamic Inactivation of Cryptococcus neoformans. Plos One, 2013. 8(1).
- Eichner, A., et al., Dirty hands: photodynamic killing of human pathogens like EHEC, MRSA and Candida within seconds. Photochemical & Photobiological Sciences, 2013. 12(1): p. 135-147.
- Teichert, M.C., et al., Treatment of oral candidiasis with methylene blue-mediated photodynamic therapy in an immunodeficient murine model. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2002. 93(2): p. 155-60.
- Huang, L.Y., et al., Progressive cationic functionalization of chlorin derivatives for antimicrobial photodynamic inactivation and related vancomycin conjugates. Photochemical & Photobiological Sciences, 2018. 17(5): p. 638-651.
- Alberdi, E. and C. Gomez, Successful treatment of Pityriasis Versicolor by photodynamic therapy mediated by methylene blue. Photodermatol Photoimmunol Photomed, 2020.
- Muller, A., et al., Electron beam functionalized photodynamic polyethersulfone membranes – photophysical characterization and antimicrobial activity. Photochem Photobiol Sci, 2018. 17(10): p. 1346-1354.
- Smijs, T.G.M., et al., Investigation of conditions involved in the susceptibility of the dermatophyte Trichophyton rubrum to photodynamic treatment. Journal of Antimicrobial Chemotherapy, 2007. 60(4): p. 750-759.
- Bornhutter, T., et al., Singlet oxygen luminescence kinetics under PDI relevant conditions of pathogenic dermatophytes and molds. J Photochem Photobiol B, 2018. 178: p. 606-613.
- Wen, X., et al., Potassium Iodide Potentiates Antimicrobial Photodynamic Inactivation Mediated by Rose Bengal in In Vitro and In Vivo Studies. Antimicrob Agents Chemother, 2017. 61(7).
- Vandresen, C.C., et al., In vitro photodynamic inactivation of conidia of the phytopathogenic fungus Colletotrichum graminicola with cationic porphyrins. Photochem Photobiol Sci, 2016. 15(5): p. 673-81.
- Preuss, A., et al., Photodynamic inactivation of biofilm building microorganisms by photoactive facade paints. J Photochem Photobiol B, 2016. 160: p. 79-85.
- Preuss, A., et al., Photodynamic inactivation of mold fungi spores by newly developed charged corroles. J Photochem Photobiol B, 2014. 133: p. 39-46.
- Lopez-Chicon, P., et al., On the mechanism of Candida spp. photoinactivation by hypericin. Photochem Photobiol Sci, 2012. 11(6): p. 1099-107.
- Gomes, M.C., et al., Photodynamic inactivation of Penicillium chrysogenum conidia by cationic porphyrins. Photochem Photobiol Sci, 2011. 10(11): p. 1735-43.
- Zerdin, K. and A.D. Scully, Inactivation of food-borne spoilage and pathogenic micro-organisms on the surface of a photoactive polymer. Photochem Photobiol, 2010. 86(5): p. 1109-17.
- Funes, M.D., et al., Photodynamic properties and photoantimicrobial action of electrochemically generated porphyrin polymeric films. Environ Sci Technol, 2009. 43(3): p. 902-8.
- Iwamoto, Y., et al., Singlet Oxygen Production and Photobiological Effects of Pinacyanol Chloride on Yeast Saccharomyces-Cerevisiae. Journal of Pharmacobio-Dynamics, 1990. 13(5): p. 316-320.
- Mothilal, K.K., et al., Synthesis, X-ray crystal structure, antimicrobial activity and photodynamic effects of some thiabendazole complexes. Journal of Inorganic Biochemistry, 2004. 98(2): p. 322-332.
- Bartusik, D., et al., Bacterial inactivation by a singlet oxygen bubbler: identifying factors controlling the toxicity of (1)O2 bubbles. Environ Sci Technol, 2012. 46(21): p. 12098-104.
- Uslan, C., et al., The synthesis and investigation of photochemical, photophysical and biological properties of new lutetium, indium, and zinc phthalocyanines substituted with PEGME-2000 blocks. J Biol Inorg Chem, 2019. 24(2): p. 191-210.
- Tan, J., et al., Inhibitory Effects of Photodynamic Inactivation on Planktonic Cells and Biofilms of Candida auris. Mycopathologia, 2019. 184(4): p. 525-531.
In hygienesensitiven Bereichen, wie z.B. dem medizinischen Umfeld oder der Lebensmittelverarbeitung spielt die Einhaltung einer möglichst geringen Keimzahl auf Oberflächen eine wichtige Rolle, da kontaminierte Oberflächen die Übertragung von Erregern ermöglichen können. Die etablierte regelmäßige Reinigung/Desinfektion kann jedoch die Rekontamination zwischen zwei Reinigungszyklen nicht verhindern. Hier helfen antimikrobiell ausgestattete Oberflächen durch ihre kontinuierliche selbsttätige Wirkung Hygienelücken zu schließen.
Der wohl wichtigste Aspekt ist, dass Nanosilber-Beschichtungen nicht auf trockenen Oberflächen wirken, da ohne Flüssigkeit kein Transport der Silberionen zu den Keimen stattfinden kann. Auch eine wissenschaftliche Studie aus 2011 belegt bereits, dass Silber nur unter feuchten bzw. nassen Bedingungen wirkt. Setzt man Nanosilber auf trockenen Oberflächen ein -diese sind die Realität- ist kein Wirksamkeit festzustellen. Falls Silber unter feuchten Bedingungen angewandt wird, erzeugt es immer noch sehr schnell Resistenzen.
Die Tests zur Wirksamkeit, werden nach der ISO 22196 unter feuchten bzw. nassen Bedingungen durchgeführt. Diese Testbedingungen werden vom VDI als unrealistisch benannt. Dyphox wird unter trockenen Bedingungen getestet und zeigt als einziges antimikrobielles Wirksystem unter trockenen Bedingungen eine (sehr gute) Wirkung.
Außerdem rät das BfR (Bundesinstitut für Risikobewertung) von dem Einsatz von Silber in verbrauchernahen Anwendungen ab. Hinzu kommt, dass Nanosilber ökologisch bedenklich ist, da es als Schwermetall dauerhaft in der Umwelt zurückbleibt.
Dyphox ist ein einfaches und effektives Entkeimungsverfahren, das aus der Natur übernommen wurde. Dyphox nutzt Licht im sichtbaren Wellenlängenbereich und aktiviert dadurch den vorhandenen Sauerstoff, z.B. aus der Raumluft. Für die Wirkung von Dyphox werden keine giftigen Biozide oder Metalle wie z.B. Silber eingesetzt.
In zwei Feldtest in zwei Krankenhäusern, über ein halbes Jahr mit 1.289 Proben, konnte das relative Risiko hoher Keimlasten auf Oberflächen um bis zu 67% (bei cfu/cm² ≤ 5,0) reduziert werden.
Zudem sank der durchschnittliche Wert von Bakterien auf der aktiven Beschichtung unter 2,5 cfu/cm², einem für Krankenhäuser wichtigen Schwellenwert.
Hohe Keimlastspitzen von bis 480 cfu/cm² traten lediglich auf unbeschichteten Oberflächen auf. Mit aktiver Beschichtung erreichten Keimlastspitzen maximal bis zu 27 cfu/cm².
Achtung: Bitte NICHT mit der von Herstellern oftmals angegeben 99,99% Verringerung von Keimen verwechseln. Siehe hierzu unseren separaten Artikel im FAQ.
- Um die Reinigung des Touchscreens vorzubereiten, schalten Sie das Gerät aus (falls möglich).
- Können Sie das Gerät nicht ausschalten, stellen Sie sicher, dass Ihre Software während der Reinigung „falsche Berührungen“ toleriert.
- Nutzen Sie nur nicht scheuernde Reinigungstücher, um ein Verkratzen des Touchscreens zu vermeiden.
- Vermeiden Sie hochkonzentrierten Alkohol (> 70%), nicht verdünntes Bleichmittel, Ammoniaklösungen oder organische Chemikalien wie Farbverdünner, Aceton, Toluol, Xylol, Propyl, Isopropylalkohol oder Kerosin. Dies kann zu Verfärbungen führen.
- Lassen Sie keine Flüssigkeiten in das Gerät oder unter die DISPLAX-Folie gelangen. Sprühen Sie das DISPLAX-Produkt nicht direkt ein. Verwenden Sie stattdessen nicht tropfende, leicht eingesprühte oder angefeuchtete Tücher.
- Wischen Sie die Oberflächen mit den entsprechenden Tüchern und den zugelassenen Reinigungsmitteln ab und lassen Sie sie trocknen.
Desinfizieren Sie Ihren DISPLAX Touchscreen
- Um die Desinfektion des Touchscreens vorzubereiten, schalten Sie das Gerät aus (falls möglich).
- Können Sie das Gerät nicht ausschalten, stellen Sie sicher, dass Ihre Software während der Reinigung „falsche Berührungen“ toleriert.
- Befeuchten Sie ein neues sauberes, nicht scheuerndes Tuch mit einem Desinfektionsmittel. Stellen Sie sicher, dass das Tuch nicht tropft. Ringen Sie es aus.
- Lesen Sie die Anweisungen des Herstellers der Desinfektionslösung sorgfältig durch.
- Viele Hersteller geben vor, dass die Oberfläche einige Minuten lang feucht bleibt, um die optimale Wirkung des Desinfektionsmittels zu erreichen.
- Wischen Sie die Oberfläche mit dem Tuch ab und lassen Sie die Oberfläche trocknen.
- Verwenden Sie für jeden Touch-Screen möglichst ein eigenes Tuch.
Folgenden Materialien dürfen Sie nicht direkt auf der Folie oder Ihrem Touch-Screen verwenden:
- K5902137 (451920612602) MDRC-1219 (TS) 18/05/2017 19 4
- Alkohol in Konzentrationen> 70%
- Methyl oder Ethyl> 35%
- Verdünner oder Benzin
- Starke Lösungsmittel
- Säuren
- Reinigungsmittel mit Fluorid
- Waschmittel mit Ammoniak in einer Konzentration> 1,6%
- Scheuermittel und Reinigungsmittel mit Schleifmitteln
DISPLAX Touch-Folien verwenden projektive kapazitive Touch-Technologie. Der Sensor befindet sich somit hinter der Scheibe. Die Reinigungs- und Desinfektionsverfahren sind unkompliziert und entsprechen der Reinigung von Glasoberflächen. Durch die Funktionalität der Scheibe, empfehlen wir jedoch, die Scheibe häufiger zu reinigen, da sie viel öfter von Menschen berührt wird.
Reinigung und Desinfektion von Oberflächen sind zwei verschiedene Schritte. Durch die Reinigung werden Schmutz, Fett, Staub und andere Verunreinigungen entfernt. Die Desinfektion ist ein separater Prozess und soll erreichen, dass Bakterien und Viren inaktiviert werden. Was Sie tun müssen, um Ihre Oberflächen zu reinigen oder zu desinfizieren ergibt sich aus Ihrem Hygienekonzept.
Reinigen Ihres DISPLAX-Touchscreens
- Um die Reinigung des Touchscreens vorzubereiten, schalten Sie das Gerät aus (falls möglich).
- Können Sie das Gerät nicht ausschalten, stellen Sie sicher, dass Ihre Software während der Reinigung „falsche Berührungen“ toleriert.
- Nutzen Sie nur nicht scheuernde Reinigungstücher, um ein Verkratzen des Touchscreens zu vermeiden.
- Vermeiden Sie hochkonzentrierten Alkohol (> 70%), nicht verdünntes Bleichmittel, Ammoniaklösungen oder organische Chemikalien wie Farbverdünner, Aceton, Toluol, Xylol, Propyl, Isopropylalkohol oder Kerosin. Dies kann zu Verfärbungen führen.
- Lassen Sie keine Flüssigkeiten in das Gerät oder unter die DISPLAX-Folie gelangen. Sprühen Sie das DISPLAX-Produkt nicht direkt ein. Verwenden Sie stattdessen nicht tropfende, leicht eingesprühte oder angefeuchtete Tücher.
- Wischen Sie die Oberflächen mit den entsprechenden Tüchern und den zugelassenen Reinigungsmitteln ab und lassen Sie sie trocknen.
Desinfizieren Sie Ihren DISPLAX Touchscreen
- Um die Desinfektion des Touchscreens vorzubereiten, schalten Sie das Gerät aus (falls möglich).
- Können Sie das Gerät nicht ausschalten, stellen Sie sicher, dass Ihre Software während der Reinigung „falsche Berührungen“ toleriert.
- Befeuchten Sie ein neues sauberes, nicht scheuerndes Tuch mit einem Desinfektionsmittel. Stellen Sie sicher, dass das Tuch nicht tropft. Ringen Sie es aus.
- Lesen Sie die Anweisungen des Herstellers der Desinfektionslösung sorgfältig durch.
- Viele Hersteller geben vor, dass die Oberfläche einige Minuten lang feucht bleibt, um die optimale Wirkung des Desinfektionsmittels zu erreichen.
- Wischen Sie die Oberfläche mit dem Tuch ab und lassen Sie die Oberfläche trocknen.
- Verwenden Sie für jeden Touch-Screen möglichst ein eigenes Tuch.
Folgenden Materialien dürfen Sie nicht direkt auf der Folie oder Ihrem Touch-Screen verwenden:
- K5902137 (451920612602) MDRC-1219 (TS) 18/05/2017 19 4
- Alkohol in Konzentrationen> 70%
- Methyl oder Ethyl> 35%
- Verdünner oder Benzin
- Starke Lösungsmittel
- Säuren
- Reinigungsmittel mit Fluorid
- Waschmittel mit Ammoniak in einer Konzentration> 1,6%
- Scheuermittel und Reinigungsmittel mit Schleifmitteln
DYPHOX-Oberflächenbeschichtungen beinhalten Katalysatoren (Photosensitoren), welche Luft-Sauerstoff in Singulett Sauerstoff umwandeln. Der Singulett Sauerstoff erzeugt ein Milieu über der Oberfläche in dem Keime nicht überleben können. Es sind kein Silber oder andere Metalle in der Beschichtung enthalten. Weiterhin liegen für DYPHOX ein Zertifikat von Dermatest mit der Bewerbung „sehr gut“ vor. sowie ISEGA-Zertifikate zur Lebensmittelunbedenklichkeit und zur Speichel- und Schweißechtheit.
Reinigung und Desinfektion von Oberflächen sind zwei verschiedene Schritte. Durch die Reinigung werden Schmutz, Fett, Staub und andere Verunreinigungen entfernt. Die Desinfektion ist ein separater Prozess und soll erreichen, dass Bakterien und Viren inaktiviert werden. Was Sie tun müssen, um Ihre Oberflächen zu reinigen oder zu desinfizieren ergibt sich aus Ihrem Hygienekonzept. Geprüfte und damit wirksame Desinfektionensverfahren werden durch das RKI in der „Liste der vom Robert Koch-Institut geprüften und anerkannten Desinfektionsmittel und -verfahren“ veröffentlicht.
Generell soll eine Oberflächenbeschichtung die Keimlast auf der Oberfläche kontinuierlich reduzieren und dadurch das Ansteckungsrisiko zwischen den Desinfektionszyklen verringern. Hierzu wurde die DYPHOX-Beschichtung unter realen Bedingungen in zwei Krankenhäusern über 6 Monate mit 1.289 Proben getestet und die Ergebnisse wurden in einer Studie veröffentlicht. Darin sehen Sie, dass das Risiko hoher Keimlastspitzen und damit auch das Ansteckungsrisiko enorm gesunken ist.
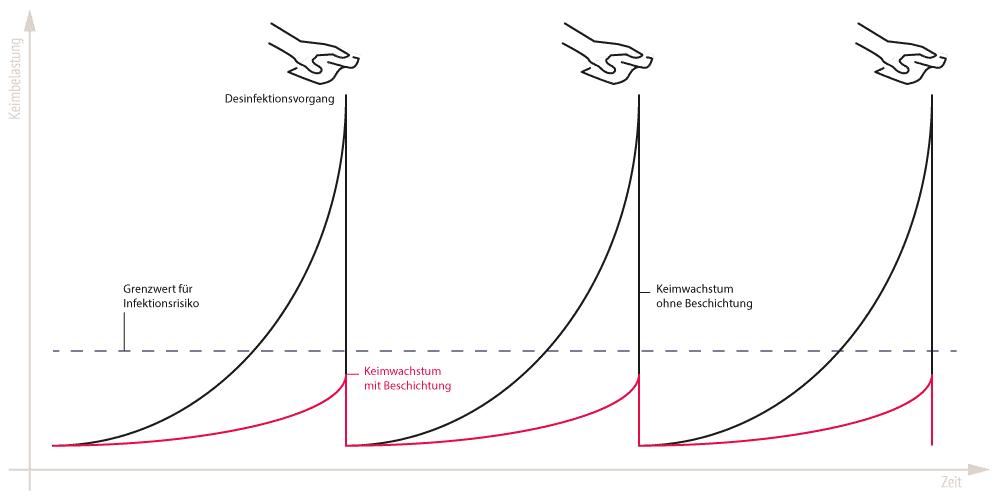
Wichtig ist, dass wir bei der Beantwortung der Fragen über eine vom RKI geprüfte Desinfektionsmethode sprechen. Eine Reinigung, auch mit schärferen Reinigern oder Reinigern mit Desinfektionsmittelzusätzen sind keine Desinfektion. Bei einer Desinfektion werden zum Beispiel die Objekte jeweils mit einem neuen Tuch bearbeitet, um eine mögliche Keimübertragung auf ein anderes Objekt zu vermeiden. Dazu werden vorgegebene Verdünnungs- und Einwirkzeiten eingehalten. Eine Desinfektion hat die Aufgabe die Keimlast auf einem Objekt vollständig zu beseitigen. Direkt nach einem Desinfektionsvorgang setzen sich wieder Keime bspw. durch absinkende Tröpfchen aus der Luft oder durch Hände-Kontakt auf Oberfläche ab und vermehren sich dort. Die Oberflächenbeschichtung sorgt für eine starke Keimreduktion zwischen den Desinfektionsintervallen. Die Keimlast bleibt niedrig. (siehe Abbildung) Das Ansteckungs- und Infektionsrisiko sinkt.
Anwendungsgrafik um Hygienelücken zwischen Desinfektionszyklen zu visualisieren. Vergleich der Keimlasten und Keimlastspitzen zwischen alleinigem Gebrauch eines Desinfektionmittels (schwarze Kurven) und der Kombination aus DYPHOX-Oberflächenbeschichtung mit Desinfektionsmittel (rote Kurven). Die Kombination aus DYPHOX und Desinfektionsmittel zeigt eine deutliche Verringerung der Keimlast und Keimlastspitzen.
Die Reduktion von Bakterien oder Viren ist nur durch eine vom RKI geprüfte Desinfektion, wie oben beschrieben sicher gestellt. Auch, weil unterschiedliche Viren und Bakterien unterschiedliche Anforderung an die Inaktivierung haben. Eine normale Reinigung reicht dafür nicht aus, da sie nur wenige oder keine Viren und Bakterien inaktiviert.
Da die normale Reinigung nur wenige Auswirkungen auf die Keime hat, können Sie diese an Ihre Bedürfnisse anpassen.
Im Gegensatz dazu sollten Sie eine Desinfektion nach den anerkannten Desinfektionsverfahren und Hygienestandards in den vorgegeben Abständen weiterhin durchführen.
Alle Keime, ob Bakterien, Viren, Pilze und Sporen, werden kontinuierlich durch die Beschichtung angegriffen. Da die Umwelt jedoch stetig Keime enthält, die sich auf Oberflächen stetig absetzen und vermehren, gibt es zeitlich betrachtet keine absolute „Keimfreiheit“.
Eine Keimfreiheit ist lediglich nach einer richtigen Desinfektion für einen Moment herstellbar oder unter Laborbedingungen.
Unter Laborbedingungen ist die antimikrobielle Oberflächenbeschichtung in der Lage 99,9 – 99,999% aller Keime zu töten. Das sind Werte mit denen andere antimikrobielle System ebenso werben. Es sind jedoch theoretische Werte, die kaum die alltägliche Situation in Krankenhäusern, Arztpraxen, MVZ etc. widerspiegeln.
Brauchbare, praxisbezogene Werte bzgl. der Reduktion von Keimlast wurden mit der antimikrobiellen DYPHOX-Oberflächenbeschichtung in Feldstudien an zwei Krankenhäusern geschaffen. Über einen Zeitraum von 6 Monaten wurden 1.289 Proben im klinischen Alltag genommen und ausgewertet. Die Ergebnisse zeigten eine Reduktion des relativen Risikos hoher Keimlasten auf Oberflächen um bis zu 67% (für cfu/cm² ≤ 5,0).
Zudem sank der durchschnittliche Wert von Bakterien auf der aktiven Beschichtung unter 2,5 cfu/cm², einem für Krankenhäuser wichtigen Schwellenwert. Beim Gebrauch von Desinfektionsmitteln ohne DYPHOX-Oberflächenbeschichtung traten hohe Keimlastspitzen von bis zu 480 cfu/cm² auf. Im Vergleich dazu verringerte die aktive DYPHOX-Oberflächenbeschichtungen die Keimlastspitzen auf einen Maximalwert von 27 cfu/cm²
Anwendungsgrafik um Hygienelücken zwischen Desinfektionszyklen zu visualisieren. Abbildung: Verringerung hoher Keimlast und Keimlasspitzen durch die antimikrobielle DYPHOX-Oberflächenbeschichtung (rote Kurven). Alleiniger Gebrauch von Desinfektionsmitteln (schwarze Kurven) führt zu höheren und schnelleren Anstiegen der Keimlast und Keimlastspitzen und somit zu einem statistisch höheren Infektionsrisiko.
Sol-Gel-Beschichtungen haben ihren Namen durch den Herstellungsprozesses (s.g. Sol-Gel-Prozess bzw. Sol-Gel-Verfahren). Bei der Sol-Gel-Beschichtung werden Dispersionen verwendet, die z.B. Alkoholate enthalten. Zuerst hydrolisieren diese Alkoholate und beginnen dann zu polymerisieren. Dabei entstehen Molekülketten und nach längerer Dauer kleinste Partikel. Ab jetzt wird diese Dispersion als Sol bezeichnet.
Nach einer entsprechenden Topfzeit, entsteht auf den Partikeln im Sol eine Art Netzstruktur und das Sol beginnt zu gelieren. Ab jetzt ist da die Beschichtung die Eigenschaften eines Gels. Dieses Gel kann durch Sprühen, Wischen oder Tauchen auf ein Objekt auftragen werden. Durch einen kurzen Sinterprozess härtet das Gel aus. So entsteht eine glasartige Schicht, die sehr kratzbeständig ist.
Grundsätzlich empfiehlt sich eine Kombination aus Reinigungs- und Desinfektionsmitteln sowie der DYPHOX-Oberflächenbeschichtung. Gerade in hochfrequentierten Bereichen treten durch den Kontakt von Personen mit Oberflächen oftmals starke, organische Verschmutzung auf. Durch eine ordentliche Reinigungsprozedur werden diese Verschmutzungen entfernt.
Die Entfernung und Abtötung von Keimen auf Oberflächen werden durch Desinfektionsmittel bewerkstelligt. Die DYPHOX-Oberflächenbeschichtung verhindert in den oftmals langen Reinigungs- und Desinfektionsintervallen das Risiko hoher Keimlast und Keimlastspitzen.
Die in Feldstudien an zwei Krankenhäusern erzielten Ergebnisse zeigen die Praxistauglichkeit der DYPHOX-Oberflächenbeschichtung auch in stark frequentierten Einrichtungen. Das Risikos einer hohen Keimlast wurde mit der Oberflächenbeschichtung auf bis zu 67% (cfu/cm² ≤ 5.0, cfu = KbE = Kolonie bildende Einheiten) reduziert. Im Vergleich hierzu konnten auf nicht beschichteten Flächen bis 480 cfu/cm² gezählt werden. Starke Personen-Frequentierungen und damit verbundene, stetige Kontaminierungen von Oberflächen scheinen der Wirksamkeit der DYPHOX-Oberflächenbeschichtung nicht entgegen zu stehen.
Bei der Beantwortung dieser Frage trifft man oftmals auf Unklarheiten. Man unterscheidet generell zwischen einer qualitativen und einer quantitativen Verringerung der Keimlast.
Die qualitative Verringerung der Keimlast sagt aus, dass bspw. 99,99% aller Arten von Keimen – bspw. S. aureus, E. coli, usw. – inaktiviert / getötet werden. Die Frage ist hierbei: Welche Keime werden getötet?
Die quantitative Verringerung der Keimlast sagt aus, dass bspw. 99,99% der Gesamtzahl aller Keime – unabhängig von einer genauen Bestimmung der Keimarten – inaktiviert / getötet werden. 99,99% entsprechen einer Verringerung um das 10.000-fache. Man spricht auch von einer Verringerung um 4 logarithmische Stufen.
Beispiel für quantitative Verringerung der Keimlast:
Eine definierte Fläche beinhaltet 1.000.000 aktive Keime. Wird bspw. durch eine antimikrobielle Oberflächenbeschichtung eine Verringerung der Keimzahl um 99,99% erreicht, dann befinden sich danach noch 100 aktive Keime auf der Oberfläche.
Hierbei handelt es sich um Laborwerte, welche alltäglichen Situationen in medizinischen Einrichtungen etc. nur sehr begrenzt widerspiegeln. Im Labor werden Faktoren wie Frequentierung von Oberflächen, organische Verschmutzungen, Aufbringung neuer Keime etc. nicht / kaum berücksichtigt.
KbE bedeutet Kolonie bildende Einheiten und ist die Übersetzung von cfu = colony forming units.
KbE / cfu bezeichnet die Anzahl von einzelnen Mikroorganismen-Zellen auf einer bestimmten Fläche, die in der Lage sind durch Zellteilung Kolonien zu bilden. Zur Quantifizierung wird standardmäßig das Verhältnis von cfu / cm² verwendet.
Beispiel: Ist die Rede von 238 cfu/cm² so sprechen wir von 238 Mikroorganismen-Zellen, beispielsweise Bakterien auf einer Fläche von 1 cm x 1 cm, einem Quadratzentimeter (cm²).
Im Gegensatz zu Bakterien, Pilzen etc. handelt es sich bei Viren um nicht-lebende Einheiten. Die Begründung dafür liegt im fehlenden Stoffwechsel sowie in der fehlenden Möglichkeit sich zu reproduzieren – Nachkommen zu bilden -. Viren brauchen dazu Wirtszellen, welche für die Vermehrung des Virus umprogrammiert / manipuliert werden.
Man unterscheidet zwischen behüllten und unbehüllten Viren sowie zwischen RNA-Viren und DNA-Viren.
Vertreter behüllter Viren sind Influenza- sowie SARS-CoV2-Viren. Rota- und Noroviren sind Vertreter unbehüllter Viren.
RNA-Viren sind bspw. Corona- und Rotaviren. Humane Papillomaviren (HPV) sowie Pockenviren zählen zu den DNA-Viren.
MDR = Multidrug Resistance Bakterien weisen Resistenzen gegenüber zahlreiche Antibiotika auf und haben zunehmend klinische Relevanz.
Ein besonderes Problem bilden MDR-Efflux-Pumpen, welche Antibiotika gezielt aus Bakterien heraus transportieren. Dadurch können Antibiotika nicht mehr in Bakterien wirken. Es bilden sich Resistenzen.
Photosensitoren sind Moleküle / Verbindungen, welche chemische und physikalische Veränderungen in einem Ziel-Molekül verursachen.
Dabei wird dem Ziel-Molekül entweder ein Elektron übertragen oder ein Wasserstoff-Ion entzogen.
Photosensitoren benutzen Lichtenergie verschiedener Wellenlängen um Ziel-Moleküle in einen höheren energetischen Zustand zu versetzen.
Diese Energie kann bspw. genutzt werden, um Luft-Sauerstoff in Singulett-Sauerstoff (¹O2) umzuwandeln.
¹O2 wiederum ist die Basis für unsere antimikrobielle DYPHOX-Oberflächenbeschichtung.
Keime sind grundsätzlich in der Luft und auf Oberflächen zu finden. Die Menge der Keime in der Luft wird durch Tröpfchen, welche durch Ausatmen und Niesen entstehen, erhöht.
Bedingt durch die Schwerkraft sinken viele Keime in der Luft und landen schlussendlich auf Oberflächen. Die Keimzahl auf Oberflächen wächst zudem durch Personenkontakt. Mit jeder Berührung von Oberflächen werden neben organischem Material Keime übertragen. Die Infektionsgefahr wächst.
Die antimikrobielle DYPHOX-Oberflächenbeschichtung basiert auf der Bildung von Singulett-Sauerstoff, welcher Viren, Bakterien und Pilze inklusive Sporen auf Oberflächen effektiv inaktiviert.
Multiresistente Keime stehen vermehrt im Zusammenhang mit dem Auftreten nosokomialer Infektionen. In einer Studie (Eichner et al. 2019) an zwei Krankenhäusern konnte gezeigt werden, dass die Anzahl multiresistenter Keime auf Oberflächen mit einer antimikrobiellen Dyphox-Oberflächenbeschichung stark verringert werden konnte. In der Folge kann somit auch das Risiko einer nosokomialen Infektion sinken.
Eine nosokomiale Infektion ist eine in Kränkenhäusern oder Pflegeeinrichtungen erworbene Infektion. Der Infektionstag, der Tag mit dem ersten Symptom, darf frühestens der 3. Tag des Krankenhausaufenthaltes sein.
Multiresistente Keime sind Mikroorganismen und Viren, welche gegen mehrere Antibiotika beziehungsweise Virostatika unempfindlich sind.
Sie werden als Superkeime bezeichnet.
Methicillin-resistenter Staphylococcus aureus (MRSA), Vancomycin-resistenter Enterokokken (VRE), Acinetobacter baumannii, Clostridium difficile, Enterohämorrhagische Escherichia coli (EHEC) etc. sind hierbei einige Beispiele.
Der Mensch, wie auch andere Organismen besitzen Photosensitoren in der Haut, welche in Gegenwart von Licht (bspw. UVA und UVB) molekularen Luftsauerstoff in Singulett-Sauerstoff umwandeln? Auf Basis unterschiedlicher Konzentrationen endogenen Singulett-Sauerstoffs werden Zellprozesse gesteuert. Singulett-Sauerstoff ist daher ein unverzichtbares Molekül für einen funktionierenden Organismus.
Quellen:
- Bäumler W, Singlet oxygen in skin: Singlet Oxygen: Applic. Biosci. Nanosci., 2016, Vol. 2, Chapt. 36
- Bäumler W et al., UVA and endogenous photosensitizers – the detection of singlet oxygen by its luminescence: Photochem. Photobiol. Sci., 2012, 11, 107-117
Es konnte gezeigt werden, dass Bacillus atrophaeus Endosporen durch Singulett-Sauerstoff inaktiviert werden.
Quelle: Eichner et al., Fast and effective inactivation of Bacillus atrophaeus endospores using light-activated derivates of vitamin B2: Photochem. Photobiol. Sci. 2015, 14, 387-396
Singulett-Sauerstoff ist ein Gas. Es unterscheidet sich durch seine höhere chemischen Reaktivität gegenüber organischen Verbindung (bspw. Zellwände und Zellmembranen) vom energieärmeren Triplett-Sauerstoff.
Die Synthese von Singulett-Sauerstoff ist ebenso im Reich der Pilze zu finden. Dabei wird Singulett-Sauerstoff beispielsweise für den Abbau von Lignin (Holz) und zur Abwehr von Feinden synthetisiert.
Quellen:
- Nakatsubo F, Reid ID, Kirk TK, Involvement of singlet oxygen in the fungal degradation of lignin, Biochem Biophys Research Comm, 102 (1), 1981: 484-491.
- Beltrán-García MJ et al., Singlet Molecular Oxygen Generation by Light-Activated DHN-Melanin of the Fungal Pathogen Mycosphaerella fijiensis in Black Sigatoka Disease of Bananas, PLOS ONE, 2014.
- Xu X, Hu X, Neill SJ, Fang J, Cai W, Fungal elicitor induces singlet oxygen generation, ethylene release and saponin synthesis in cultured cells of Panax ginseng C. A. Meyer, Plant Cell Physiol, 2005, 46(6): 947-954.
Synthetisiert auf Oberflächen von Pflanzenblättern durch den Prozess der Photosensitization wird Singulett-Sauerstoff an die Luft abgegeben. Daher atmen wir jeden Tag moderate Konzentrationen Singulett-Sauerstoff ein.
In Säugetieren gibt es ebenfalls Photosensitizer, darunter Vitamine, welche endogen Singulett-Sauerstoff produzieren. (Bäumler, 2016)
W. Bäumler. Endogenous Singlet Oxygen Photosensitizers in Mammalians (2016) Singlet Oxygen: Applications in Biosciences and Nanosciences, Volume 1, 239-269.
Mikroorganismen können physikalisch sowie chemisch inaktiviert werden.
Physikalische Inaktivierung wird beispielsweise durch Erhitzen – Sterilisieren, Pasteurisieren – oder durch UVC-Strahlung gewährleistet. Dabei werden die Mikroorganismen irreversibel beschädigt und sterben.
Mit der chemischen Inaktivierung durch Antibiotika oder Konservierungsmittel wird das Wachstum und Reproduktion von Mikroorganismen unterbunden.
Die Inaktivierung von Mikroorganismen durch die Singulett-Sauerstoff produzierende Oberflächenbeschichtung DYPHOX kann man als chemisch-physikalische Inaktivierung betrachten. Der Singulett-Sauerstoff oxidiert Strukturen der Zellwand und Zellmembran, welche dort zu Brüchen führt. Die Mikroorganismen verlieren ihre Integrität und sterben.
Einen Zustand der Keimfreiheit wird auf Oberflächen direkt nach der Desinfektion mit geeigneten Desinfektionsmitteln erreicht.
Bereits nach kurzer Zeit sammeln sich Keime / Mikroorganismen durch Kontakt zu Menschen oder in der Luft absinkende Tröpfchen auf dieser Oberfläche an und können exponentiell wachsen. Dadurch nimmt die Keimzahl explosionsartig zu. Das Infektionsrisiko steigt.
Eine antimikrobielle Oberflächenbeschichtung verhindern einen exponentiellen Anstieg der Keimzahl zwischen den Desinfektionszyklen und verringern somit das Risiko hoher Keimlastspitzen nachweislich. (Eichner et al., 2020)
Quelle: A Eichner, T Holzmann, D B Eckl, F Zeman, M Koller, M Huber, S Pemmerl, W Schneider-Brachert, W Bäumler: Novel photodynamic coating reduces the bioburden on near-patient surfaces thereby reducing the risk for onward pathogen transmission: a field study in two hospitals. 2020 J Hosp Infect 104(1): 85-91.
Die Übertragung von Mikroorganismen und Krankheitserregern über Oberflächen beschreibt alltägliche Situationen.
Zur Kontrolle der Keimbelastung auf Oberflächen werden oftmals Abklatschtests verwendet.
Die Probenentnahme auf Oberflächen kann einige Fehlerquellen beinhalten. Diesbezüglich ist eine Standardisierung unverzichtbar.
Wichtige Eckpunkte und Fragen der Probeentnahme sind: Handelt es sich um gleiche Zeitpunkte der Probenentnahme? Wurde ein standardisierter Anpressdruck verwendet? Sind antimikrobiell beschichtete und unbeschichtete Oberflächen bzgl. Frequentierung, Biofilm, Lichtverhältnisse usw. vergleichbar?
Fehlende Standardisierungen führen in der Folge zu großen Schwankungen sowie Standardabweichungen und somit zu wenig aussagekräftigen Ergebnissen. Falsche Schlussfolgerungen können die Folge sein.
Grundsätzlich verfolgen beide Ansätze eine signifikante Keimreduktion.
Die Strategie ist dabei sehr unterschiedlich und richten sich nach den vorhandenen Bedingungen.
Auf trockene Oberflächen, welche im Kontakt mit Menschen stehen und / oder in der Lebensmittelindustrie eingesetzt werden können, empfiehlt sich beispielsweise eine antimikrobielle Oberflächenbeschichtung.